臨床医学研究
臨床医学研究について
京都大学医学部附属病院腫瘍内科は、実施している臨床試験の数が院内で一二を争うほど多い診療科です。また、次世代医療・iPS細胞治療研究センター(Ki-CONNECT)と連携する主要な診療科としても精力的に臨床試験を行っています。
臨床試験
当科では、特定臨床研究や観察研究、先進医療制度を利用した臨床研究、さらには医師主導治験や企業治験まで数多くの臨床試験を行っています(表参照)。食道がんや膵がん、がんゲノム医療については、多施設共同試験の主施設として医師主導治験や先進医療臨床試験を主導しています。 JCOGやWJOGなど国内臨床試験グループの多施設共同試験にも参加し、日常診療を進歩させるエビデンスの創出に貢献しています。
当科で実施中の臨床試験の数(2022年1月時点)
| 特定臨床研究・観察研究 | 先進医療 | 医師主導治験・企業治験 |
|---|---|---|
| 34 | 1(主施設) | 16 |
以下に、当科が主たる施設として行った先進医療研究および治験について代表的なものを記載します。
先進医療B(申請医療機関:京都大学医学部附属病院腫瘍内科)
| 「化学療法未施行の切除不能進行・再発固形がんに対するマルチプレックス遺伝子パネル検査の有用性評価に関する臨床研究(FIRST-Dx trial)」 | |
| 実施機関 | 京都大学(主施設)、東京大学、東京医科歯科大学、愛知県がんセンター、富山大学、和歌山県立医科大学(順不同) |
| 症例集積期間 | 2021年5月~2022年2月。 登録症例数:180例(完了)。 |
| 研究概要 | 全身化学療法未施行の切除不能進行・再発がん症例において、FoundationOne® CDxがんゲノムプロファイル検査を用いてコンパニオン診断を含むActionable/Druggableな遺伝子異常を有する症例の割合を求めることで、初回治療法選択における遺伝子プロファイルリング検査の臨床的有用性を検証します。詳細は次項「がんゲノム医療とがん遺伝子パネル検査の活用について」に記載しています。 |
多施設共同医師主導治験
| 「食道がん患者を対象とした根治的化学放射線療法とNivolumab併用による探索的多施設共同非盲検医師主導治験(NOBEL trial)」 | |
| 実施機関 | 京都大学(主施設)、千葉県がんセンター、 国立がん研究センター中央病院、 国立がん研究センター東病院(順不同) |
| 症例集積期間 | 2019年1月~。 登録症例数:60例(完了)。 |
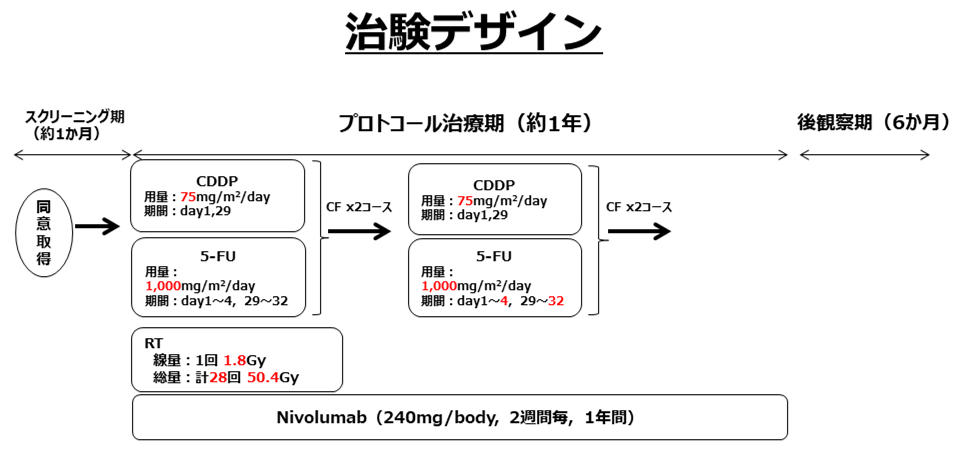
| 研究概要 | 食道がんに対する化学放射線療法は、非外科的な治療として、唯一の根治治療である。この根治的化学放射線療法に免疫チェックポイント阻害薬であるNivolumab を同時併用+維持療法を実施することで、抗腫瘍効果のさらなる向上を期待した医師主導治験を実施しています(図参照)。本治験では、治療の有効性・安全性を評価し、同時にバイオマーカーを探索する計画です。 |
多施設共同医師主導治験
| 「食道がん化学放射線療法後の局所遺残再発例に対するME2906およびPNL6405EPGを用いた光線力学療法の多施設共同臨床第II相試験」 | |
| 実施機関 | 京都大学(主施設) |
| 研究概要 | 食道がんに対する化学放射線療法または放射線療法後の局所遺残再発例に対するタラポルフィンナトリウム(ME2906)およびPDT半導体レーザ(PNL6405EPG)を用いた光線力学療法の有効性と安全性を医師主導治験で検証し、主要エンドポイントである原発巣の完全奏効率は、88.5%でした。本試験の結果、本薬剤および医療機器は厚生労働省から薬事承認を得て、現在臨床応用されています。 |
- 論文発表:Yano T, et al. A multicenter phase II study of salvage photodynamic therapy using talaporfin sodium (ME2906) and a diode laser (PNL6405EPG) for local failure after chemoradiotherapy or radiation for esophageal cancer. Oncotarget 2017;8(13): 22135-22144.
多施設共同医師主導治験
| 「多剤不応進行再発食道がんに対するFTD/TPI合剤(TAS-102)の有効性および安全性に関する第Ⅱ相臨床試験」 | |
| 実施機関 | 京都大学(主施設) |
| 研究概要 | 5FU,プラチナ製剤,タキサン系製剤に不応もしくは不耐となった患者を対象に、FTD/TPI合剤の有効性と安全性を検討した臨床試験です。 |
- 論文発表:Mori Y, et al. Multicenter phase II study of trifluridine/tipiracil for esophageal squamous carcinoma refractory/intolerant to 5-fluorouracil, platinum compounds, and taxanes: the ECTAS study. Esophagus 2022 in press.
多施設共同臨床研究
| 「難治性食道がんの治療方針決定に資する技術開発に関する研究(SUitable Classification Consortium for Esophageal Squamous cell carcinoma Subtype: SUCCESS試験)」 | |
| 実施機関 | 京都大学(主施設) |
| 研究概要 | 内視鏡下に生検した食道がん組織の遺伝子発現解析を行い、そのプロファイリング結果に基づき食道がんのサブタイプ分類を行い、各サブタイプ群の化学放射線療法, 外科治療に対する治療効果・予後を検討し、根治性の高い個別化医療を実現するための革新的バイオマーカー開発を目指す研究です。(本試験をもとに、プログラム医療機器として薬事承認申請予定。) |
医師主導治験
「呼気中のアセトアルデヒド/エタノール比を用いた低侵襲迅速ALDH2遺伝子型判別法の開発」
- 論文発表:Aoyama I, et al. Establishment of a Quick and Highly Accurate Breath Test for ALDH2 Genotyping. Clin Transl Gastroenterol. 2017; 8(6): e96.
多施設共同観察研究
| 「呼気中アセトアルデヒド/エタノール濃度比と頭頸部・食道がん発症リスクの関連性に関する研究(Breath AERO-E study)」 | |
| 実施機関 | 京都大学(主施設)、国立がん研究センター東病院、国立がん研究センター中央病院、石川県立中央病院、鹿児島大学、北里大学、岡山大学、熊本大学 |
| 症例集積期間 | 2019年11月26日~2024年11月25日。 登録症例数:315例 |
| 研究概要 | 本研究は、頭頸部・食道がんのリスクを調べる新たな手段として、少量のエタノール摂取後の呼気ガスから算出されるアセトアルデヒドとエタノールの濃度比(A/E比)の有用性を明らかにし、頭頸部・食道がんのハイリスクであるALDH2*2多型保有者をスクリーニングする非侵襲的迅速測定法の開発を目的としています。 |
がんゲノム医療とがん遺伝子パネル検査の活用について
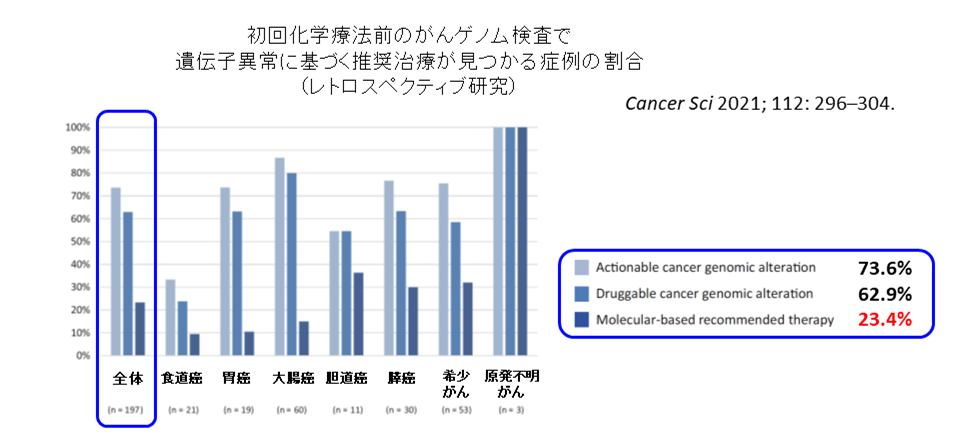
当科ではがん遺伝子パネル検査が国内保険承認となる以前から、がん遺伝子パネル検査を用いた臨床研究に取り組んできました(Cancer Sci 2017; 108: 1440-1446.)。その後2019年に保険承認されましたが、その対象は「標準治療がない、もしくは終了した症例」に限られており、検査をしても全身状態が悪いため治療にまでつながらない症例が多いことが臨床現場では問題となっています。我々は、がん遺伝子パネル検査をがんの初回診断時に行うことの有用性を示すために、後ろ向き観察研究を行いました(Cancer Sci 2021; 112: 296–304.)。その結果、約60%の症例で治療につながる可能性のある遺伝子異常が検出され、全体の23.4%で実際に治療薬を提案可能であることを報告しました(図参照)。2021年には、がん遺伝子パネル検査の保険適応拡大を目指し、がんの初回診断時にがん遺伝子パネル検査を行う前向き多施設共同臨床試験を先進医療Bの枠組みで主導しました(告示番号B71;UMIN000042408「化学療法未施行の切除不能進行・再発固形がんに対するマルチプレックス遺伝子パネル検査の有用性評価に関する臨床研究(FIRST-Dx trial)」。「臨床試験」の項参照)。
- 論文発表:Kondo T, et al. Comprehensive genomic profiling for patients with chemotherapy-naïve advanced cancer. Cancer Sci 2021; 112(1): 296-304.
Kou T, et al. Clinical sequencing using a next-generation sequencing-based multiplex gene assay in patients with advanced solid tumors. Cancer Sci 2017; 108(7): 1440-1446.